Photocatalyse : Différence entre versions
(→Définitions) |
(→Caractèristiques techniques) |
||
| Ligne 14 : | Ligne 14 : | ||
| − | Le catalyseur le plus utilisé est le dioxyde de titane TiO2) car thermodynamiquement | + | Dans le cas des enduits photocatalytiques, Le catalyseur le plus utilisé est le dioxyde de titane TiO2) car thermodynamiquement stable, non toxique et économique. <br /> |
| − | stable, non toxique et économique. En exposant ce catalyseur et semi-conducteur à la | + | En exposant ce catalyseur et semi-conducteur à la lumière comportant un composant UV, une activation a lieu. Cette énergie peut à son |
| − | lumière comportant un composant UV, une activation a lieu. Cette énergie peut à son | + | tour enclencher d’autres processus, tels que des réactions redox et des transformations moléculaires, avec des matières présentes dans l’atmosphère environnante. |
| − | tour enclencher d’autres processus, tels que des réactions redox et des transformations | ||
| − | moléculaires, avec des matières présentes dans l’atmosphère environnante. | ||
La réaction photocatalytique a lieu à la surface du matériau et se déroule en plusieurs phases. <br /> | La réaction photocatalytique a lieu à la surface du matériau et se déroule en plusieurs phases. <br /> | ||
Version du 16 mai 2008 à 16:24
Sommaire
Définitions
Revêtement réalisant la photocalyse lui conférant des propriétés auto-nettoyantes et dépolluantes
La photocatalyse est le phénomène naturel dans lequel une substance, appelée photocatalyseur, accélère la vitesse d’une réaction chimique sous l’action de la lumière (naturelle ou artificielle).
Lors de cette réaction, le catalyseur n’est ni consommé ni altéré. Cette réaction présente beaucoup de similitude avec la synthèse chlorophyllienne.
En utilisant l’énergie lumineuse, l’eau et l’oxygène de l’air, les photocatalyseurs engendrent la formation de molécules très réactives (appelées radicaux libres), capables
de décomposer certaines substances, organiques et inorganiques, présentes dans l’atmosphère et parfois nocives, en composés totalement inoffensifs par oxydo-réduction.
Caractèristiques techniques
Dans le cas des enduits photocatalytiques, Le catalyseur le plus utilisé est le dioxyde de titane TiO2) car thermodynamiquement stable, non toxique et économique.
En exposant ce catalyseur et semi-conducteur à la lumière comportant un composant UV, une activation a lieu. Cette énergie peut à son
tour enclencher d’autres processus, tels que des réactions redox et des transformations moléculaires, avec des matières présentes dans l’atmosphère environnante.
La réaction photocatalytique a lieu à la surface du matériau et se déroule en plusieurs phases.
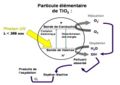
Par l’action de la lumière du soleil sur le semi-conducteur (TiO2) se forment des paires électron-trou.
Ces électrons-trous peuvent ou bien se recombiner, ou bien rester séparés par l’adsorption d’autres
matières à la surface (polluants). Des réactions d’oxydation et de réduction peuvent ensuite se produire
entre les électrons capturés et les polluants adsorbés. Les produits formés peuvent être évacués par les
eaux de pluie et/ou passer dans l’atmosphère.
La surface est ainsi efficacement nettoyée, on parle de surfaces autonettoyantes. Le TiO2 même ne participe
pas à la réaction et ne se décompose donc pas. Tant qu’il est en contact avec la lumière et les polluants,
il reste stable et efficace. La photocatalyse hétérogène utilisant du TiO2 comme photocatalyseur minéralise
un très large éventail de composés organiques (alcanes, alcènes, alcools, pesticides, etc.). Il est également
possible de réduire ou d’oxyder plusieurs autres produits (NOx, bactéries, virus, pollens, acariens, etc.).
La vitesse à laquelle ces réactions ont lieu dépend de l’intensité de la lumière, de la quantité de TiO2 en
surface et de la durée du contact entre le TiO2 et les matières présentes dans l’air.